Investigadores del IBR descubrieron un mecanismo específico que usa esa bacteria para proteger su envoltura celular en ambientes hostiles, como los encontrados durante la infección.
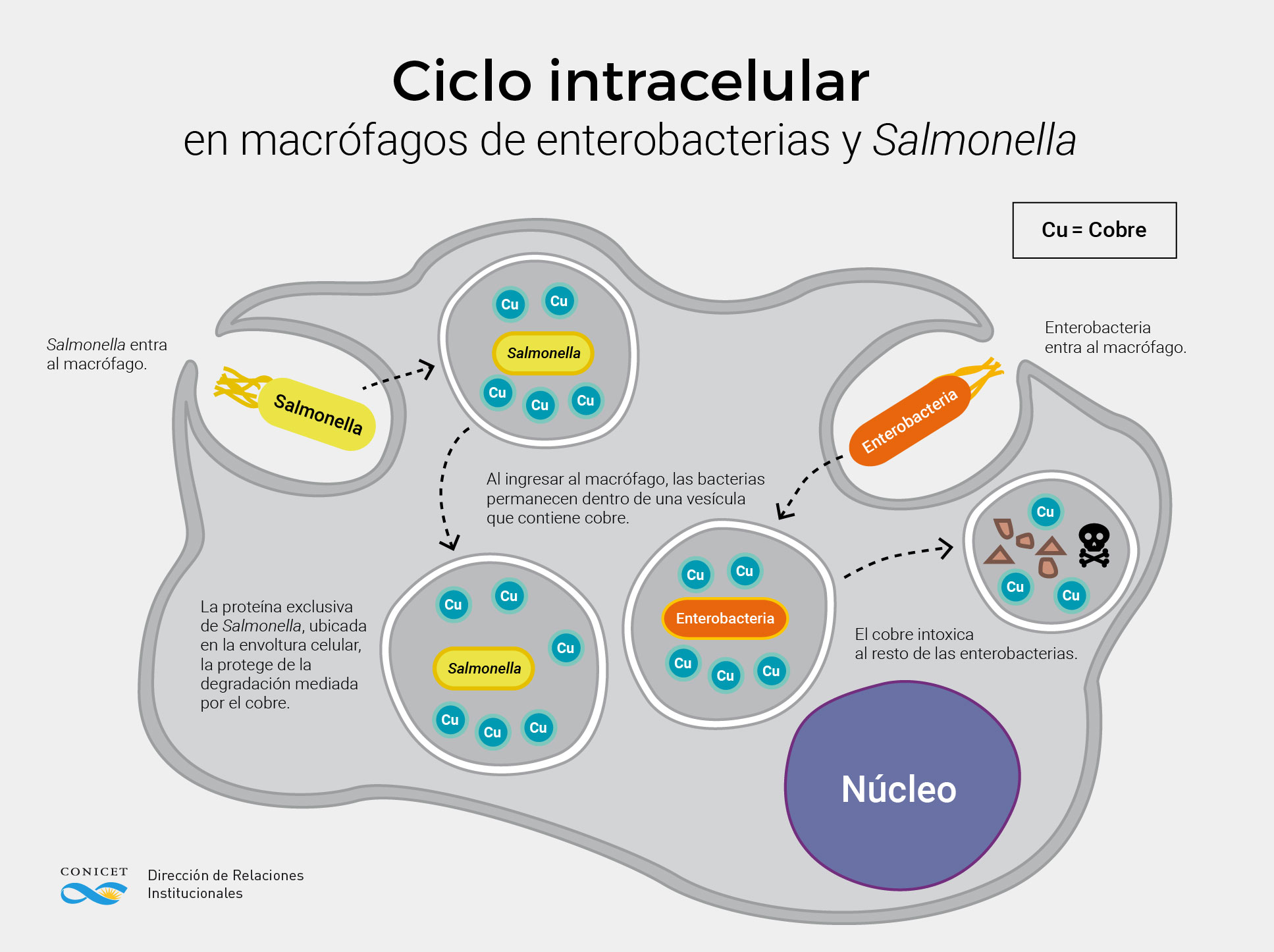
Cuando las células del sistema inmune humano detectan microorganismos invasores los eliminan mediante un proceso llamado fagocitosis, durante el cual las células internalizan – ‘meten’ en su interior – estos microorganismos, en compartimentos específicos denominados fagolisosomas, para su posterior inactivación, degradación y muerte.
Uno de los mecanismos que usan las células del sistema inmune para limitar el crecimiento de las bacterias es eliminar las cantidades de hierro y zinc, elementos que el patógeno necesita para crecer. Al mismo tiempo, el ambiente donde se encuentra la bacteria se enriquece en cobre, que actúa como agente intoxicante, un fenómeno conocido como inmunidad nutricional.
En los últimos años se demostró que el cobre juega un papel fundamental en el proceso de inactivación de bacterias, y que patógenos como Salmonella desarrollaron herramientas para limitar el efecto tóxico de este metal, poder prosperar dentro de la célula infectada y continuar así con el proceso infeccioso.
“Estudiamos como Salmonella enterica controla los niveles de cobre y vimos que usa un mecanismo muy diferente al de bacterias similares. En la mayoría de ellas hay un sistema especial de reconocimiento y de eliminación del exceso de cobre. En Salmonella ese sistema ancestral se perdió, y sabemos que estuvo porque quedó una cicatriz que muestra que esos genes estuvieron en algún momento en su genoma”, explica Fernando Soncini, investigador principal del CONICET en el Instituto de Biología Molecular y Celular de Rosario (IBR, CONICET-UNR).
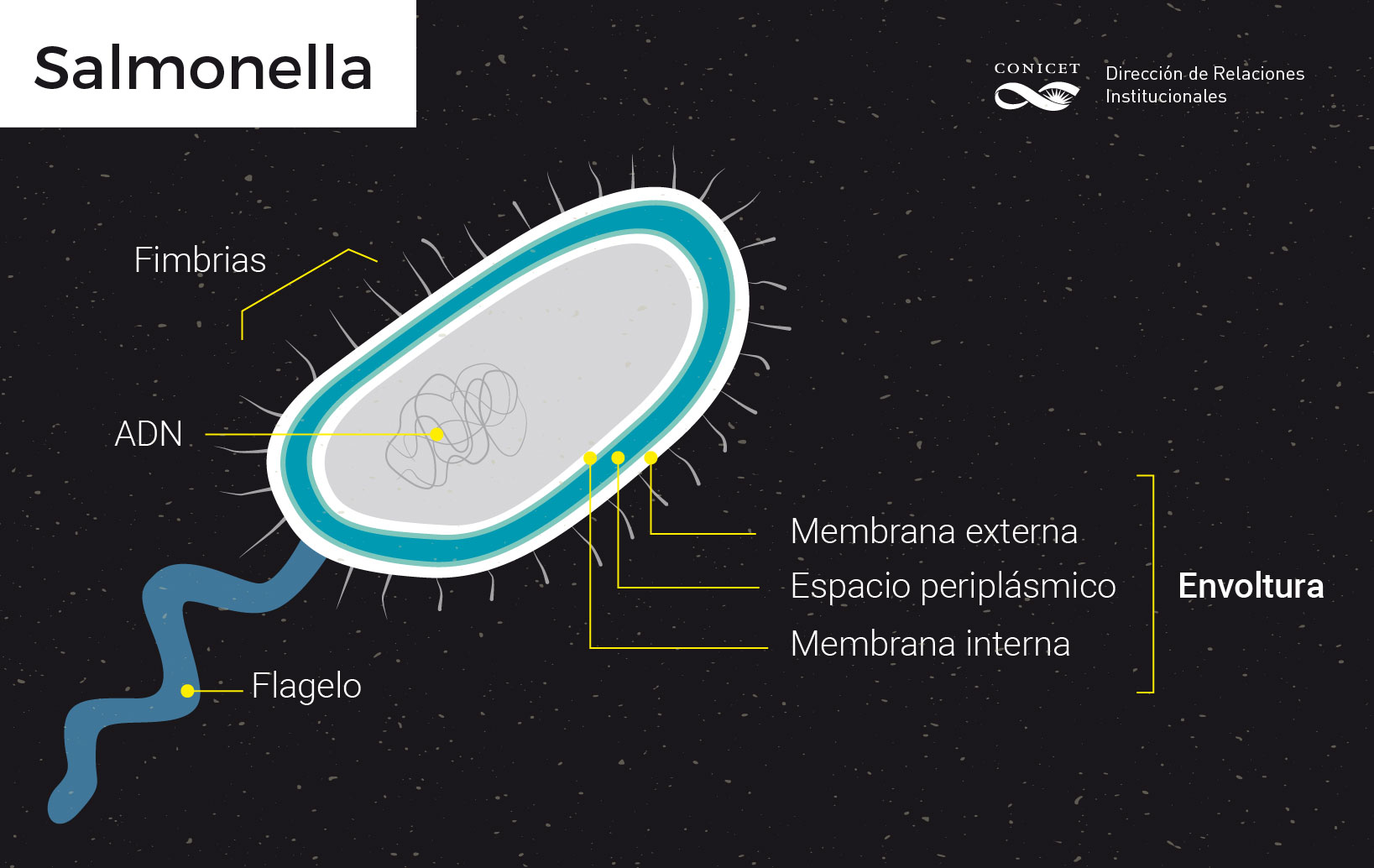
A diferencia de los organismos eucariotas, las bacterias no tienen núcleo. Las de tipo Gram negativas, como Salmonella enterica, tienen además el espacio periplasmático, que está comprendido entre la membrana plasmática y la membrana externa. Estos elementos en conjunto forman la envoltura celular.
Soncini junto a su equipo del Laboratorio de Transducción de Señales en Bacterias Patógenas del IBR, publicaron en la prestigiosa revista PNAS un estudio en el que descubrieron una proteína exclusiva de Salmonella, ubicada en la envoltura celular, que disminuye el efecto tóxico del cobre. Esto favorece la adaptabilidad y supervivencia de la bacteria a diversos tipos de entornos.
El investigador aclara que Salmonella detecta tanto la presencia de cobre como el daño que éste causa en la envoltura celular y como respuesta coordina la síntesis de una proteína que controla las concentraciones de este metal en la envoltura bacteriana. Esta regulación es esencial para que la bacteria sobreviva a un rápido incremento de cobre pero no produzca esta proteína en ambientes donde no la necesita.
“Salmonella adquirió el gen que codifica para esta proteína que le sirve tanto para el control del equilibrio de cobre en la envoltura, como para la virulencia. Este estudio, primero nos permite entender la fisiología de esta bacteria y qué necesita para ser patógeno. Segundo, hablamos de un gen que específicamente le sirve para ser patógeno y que no está presente en otras enterobacterias y por lo tanto es un buen candidato para el desarrollo de métodos terapéuticos contra Salmonella enterica”, concluye Soncini.
La infección por Salmonella produce una enfermedad diarreica conocida como salmonelosis. La bacteria vive en el intestino humano o animal y se transmite a otras personas por el contacto con heces contaminadas. La mayoría de los casos de esta enfermedad se producen por el consumo de alimentos de origen animal contaminados.
Los síntomas de la enfermedad aparecen entre las 12 y las 72 horas posteriores a la infección y son:
Diarrea.
Fiebre.
Deshidratación.
Dolor abdominal.
Dolor de cabeza.
Dolor muscular.
Gastroenteritis.
Por Cecilia Leone.
Sobre investigación:
Fernando Soncini. Investigador principal. IBR.
Carolina López. Becario Doctoral. IBR.
Alejandro Pezza. IBR.
Lucas Pontel. IBR.